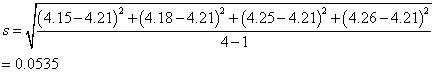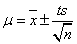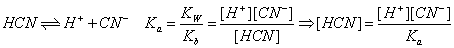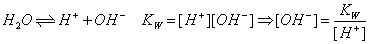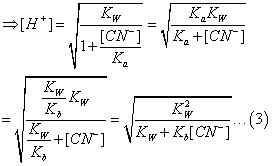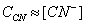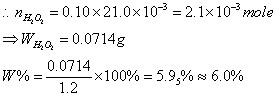考古题详解:104年公务人员高等考试3级考试试题-农畜水产品检验、商品检验-分析化学(包括仪器分析)
一、有一位检验员重复量测四次萝卜干中苯甲酸的含量(mg/Kg),得到如下数据:4.15、4.18、4.25、4.26,经查表在自由度(degrees of freedom)为3 及95%可信系数(probability level)条件下,其t-值为3.18,试计算此量测在95%的信赖范围(confidence intervals)?
解:
又信赖范围(confidence intervals, CI)之公式
where s is the measured standard deviation, n is the number of observations, and t is Student’s t value under certain probability.
<Note>
The confidence interval is an expression stating that the true mean, m , is likely to lie within a certain distance from the measured mean, 
二、试计算 0.0500M KCN 水溶液之pH 值?Kb = 2.1 × 10-5。
解:
考虑质量平衡
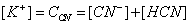
考虑电荷平衡
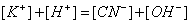
(1)带入(2)可得
∵Kb << 0.0500M KCN ∴假设
三、试说明以 EDTA 测定水中钙镁硬度时,(一)为何以缓冲溶液调pH 值?(二)为何在EDTA 滴定前,常需加入数滴KCN 水溶液?
EDTA 与Ca2+生成常数log Kf = 10.69、与Mg2+生成常数log Kf = 8.64。
解:
1. 在 EDTA 滴定法中常加入碱性缓衡溶液(氯化铵+氨水)以控制 pH 值在 10左右,因为 pH 值太高会产生氢氧化物沈淀(Mg(OH)2(s)沈淀),造成实验误差。
2. 氰化物的使用目的:有些金属離子会使滴定终点褪色、不明显或消耗EDTA,而造成干扰,因此滴定前加入特定的抑制剂,将可减少此干扰。
<Note>
EDTA 滴定时所用的指示剂称为金属指示剂,是依金属浓度而改变颜色,所用的指示剂亦为螯合剂,可与金属离子生成错合物,但稳定度较EDTA与金属离子形成的错合物低。因此加入 EDTA于金属溶液时,EDTA逐渐取代指示剂并与金属结合,在滴定终点时指示剂完全被置换出来,而显示出指示剂本身的颜色(EDTA的错合物为无色)。由于 Ca-EDTA错合物较 Mg-EDTA错合物安定,但没有 Mg2+共同存在时,Eriochrome Black T(简称 EBT)指示剂的颜色变化会不敏锐,因为 Mg2+与 EBT 指示剂形成的错合物稳定性大于 Ca2+与 EBT 指示剂形成的错合物,可使达到滴定终点的颜色变化更为明显;因此在滴定时,加入适量之 Mg2+,使 EBT 指示剂的颜色变化较为敏锐,最后再扣除 Mg2+的含量即可。
四、市面上销售使花色衣服不致于褪色之鲜艳漂白水,其主要漂白成分为双氧水。为测定其含量,取1.20 克样品,在过量的碘化钾酸性溶液中,共耗用0.10 N 硫代硫酸钠水溶液21.0 mL滴定所生成的碘分子至终点,试问:
(一)此滴定常选用的指示剂为何?使用时机?为什么?
(二)样品中双氧水的含量有多少%?
解:
1. 使用淀粉溶液作为指示剂;当溶液出现黄色时加入淀粉溶液;系因淀粉溶液可与碘形成蓝黑色错合物,当加入硫代硫酸钠溶液至碘被反应完全时,溶液成无色。
2. 利用双氧水的当量数=I2当量数=Na2S2O3当量数,计算得知未知物双氧水的含量。
<Note>
碘量法或称碘量滴定法是一种分析化学中常用到的滴定方法,同时也是一种氧化还原滴定的方法,碘量法中,通过碘单质的生成或者反应完全作为滴定终点的现象。碘量法分为间接碘量法和直接碘量法,间接碘量法通过与被分析物反应释放出的碘滴定,而直接碘量法使用碘单质滴定。经常被用来测定水溶液中氧化剂的浓度,比如生态研究中的测定溶解氧含量或者例如游泳池中活性氯的浓度。首先需要知道样品溶液的体积,再加入过量且量已知的碘化物溶液,样品中的氧化剂将碘离子氧化为碘单质,碘单质溶于含碘化物的溶液生成I3-,溶液最终变为深褐色。之后,含I3-的溶液用标准硫代硫酸钠溶液滴定,并且以淀粉为指示剂,以此计算出之前生成的I3-的量,间接地计算出之前的氧化剂的量。当溶液深蓝色消失时,意味著碘单质已被完全反应,即到达了滴定终点。
五、在电化学分析技术里,为何剥除法比其它伏安法具较佳的量测感度?
解:
阳极剥除伏安法,先进行沉积步骤,此时微电极作为阴极,测量沉积在电极上分析离子,再进剥除步骤,此时微电极作为阳极,分析物被重新氧化回原来离子状态,并记录两步骤之伏安谱。在沉积步骤中,电极表面分析物浓度远大于其在溶液的浓度,含有前浓缩之程序,因此在所有电化学分析法中,电极剥除法具有最低侦测极限值,灵敏度最大。
六、 (一) 试说明气相层析法(GC)最常使用的热传导侦测器(Thermal conductivity detector,TCD),火燄离子化侦测器(Flame ionization detector, FID)及电子捕捉侦测器(Electron capture detector, ECD)之侦测原理。
(二) 为何ECD 常被选为有机卤化物(Organic halides)之侦测器?
(三) 为何FID 常被选为碳氢化合物(Hydrocarbons)之侦测器?
解:
GC的检测器依讯号产生方式可分成全侦测器与选择性侦测器两类,全侦测器能侦测所有物质,最常使用的有TCD(Thermal Conductivity Detector)及FID(Flame Ionization Detector)。选择性侦测器能侦测到特定的物质,如对卤素有特别高感度的ECD(Electron Capture Detector),对硫、磷(金属元素)有高感度的FPD(Flame Photometric Detector)。
故本题
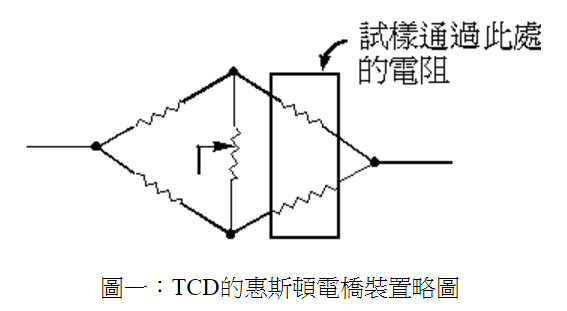
1. 热传导侦检器(Thermal conductivity detector,TCD)
TCD的设计是利用一惠斯顿电桥的装置(上图),在上侧的两股串联电阻丝之右侧电阻让不含试样的携带气体通过,做为比较用,在下侧右方的电阻丝则让携带试样的气体通过,电流通过时电阻丝会生热,通过的气体会导热,具有散热功能,在固定的电压下以及固定的气体流速下,电阻丝的温度会达到一平衡温度,当通过两侧电阻丝的气体都不含试样时,位于惠斯顿电桥中央的架桥电阻丝之中间位置可找到一零电位点,当某一侧通过两股串联电阻丝之气体中含有试样时,因为改变了气体的导热系数,致使两侧电阻丝温度不同,电阻产生变化,因此就改变了架桥电阻丝两端的电位,零电位点的位置产生偏动,于是讯号产生。
由于TCD的运作原理,倚赖携带气体的导热能力,导热系数很大的氢气及氦气为最理想的选择,因为灵敏度高,不过前者较具危险性,使用要小心,后者则很贵,各有缺点。氮气的导热系数低,因此灵敏度低,并不是理想的选择,不过它很便宜又安全,也具优点,大部份的有机化合物导热系数都不高,因此氢气或氦气参杂入有机化合物时造成的导热系数落差会很大,此为其灵敏度高的原因,产生的讯号均为同一方向的,但若用氮气为携带气体时,因为其导热系数与有机化合物相近,掺杂入其它的有机化合物时,造成的导热系数之改变有正亦有负,所以会产生正向或负向的讯号。
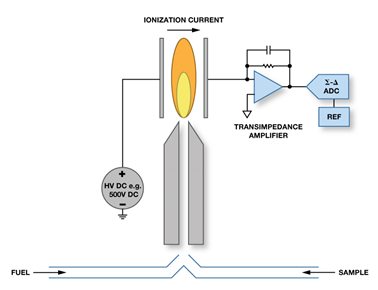
2. 火燄离子化侦测器(Flame ionization detector, FID)
利用氢气与空气之燃烧并游离自层析管住流出之分析物,产生的离子被带入收集器,吸附而产生微小的电流讯号(配合放大器),装置图如下;其优点为灵敏度高、较广的线性范围,缺点系对样品具破坏性、较热传导侦侧器昂贵,对有机物皆可检出,惟对H2O、CO2、SO2、NOx不灵敏。
碳氢化物在火焰中的游离,产生的离子数目与在火焰中碳原子被还原的数目成比例;但若含羰基(carbonyl group)、醇(alcohol group)、卤素(halogen)及胺(amine group)的官能基者因不易被还原,于FID产生离子讯号较少,没有一般FID对碳氢化物灵敏。
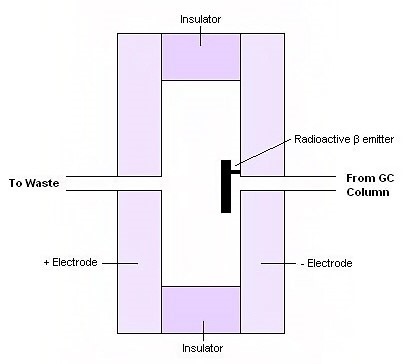
3. 电子捕捉侦测器(Electron capture detector, ECD)
电子捕捉侦侧器系为气相层析上具灵敏度且为一选择性很强的侦测器,原理为侦测器内放射性同位素(如63Ni)所释放出来的b粒子会与层析管柱中的载流气体(carrier gas,具低游离能)碰撞产生低能量的热电子(thermal electron),反应方程式如下:
b-+carrier gas → ne-+正离子+自由基+b'-(较低能量)
热电子经由侦测器内阳极的收集而产生一稳态电流,若任何易捕捉热电子之物质(电负度大的物种如卤素)随载流气体自管柱进入侦测器内则会造成稳态电流的减弱,而可作为此类物质的定量测定。
ECD其感应具有选择性,对于含卤素、过氧化物(peroxides)、对苯二酮(quinones)及硝基(nitro group,─NO2)等阴电性官能基有很高的灵敏度;对于胺、醇及烃类等化合物不灵敏。EC重点应用为环境中的多氯联苯(polychlorinated biphenyls,PCBs)、有机氯农药与饮用水中的三卤甲烷含量等的测定。
<Note>
光游离侦测器(Photo Ionization Detector, PID):光游离侦测器以9~12 eV的紫外光来游离化学物质,产生游离电子,而这些被游离出来的电子则被具正电荷的接收器所收集,产生电流讯号的改变。一般而言,光游离侦测器的大都应用于芳香族的有机物上。
七、试解释在以质谱鉴定分析物时,以化学离子化(chemical ionization)产生之图谱(mass spectrum)与电子撞击离子化(electron impact ionization)产生之图谱相较,有何特点?
解:
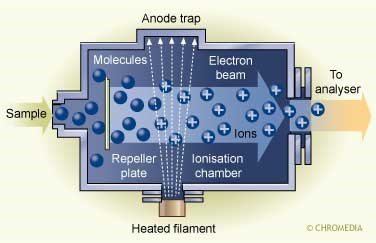
(一) 电子撞击游离法(electron impact ionization, EI)
适用于具挥发性且热稳定性高的待测物,游离方式如下图,利用经加热的灯丝(Filament)释放出电子,在外加电场的作用下使之成为带有高能量的电子(70eV),并令其撞击气态待测物,使待测物游离,游离过程中生成分子离子(Molecular ion)或碎片离子(Fragment ions),在电场的作用下分子离子或碎片离子经聚焦片(Extraction plates)与出口狭缝(Exit slit)聚焦导入质量分析器内,得到质谱图。
正常情况下,EI生成正离子的数目为负离子的1000倍,故一般探讨正离子为主。值得注意的是,用于使待测物游离的电子所具有之能量,应至少等于待测物的游离电位才能使待测物游离,惟此时的游离效率低,为了获得再现性高的质谱图,用于撞击的电子能量设定为70eV,缺点是较高的电子能量将造成分子离子的裂解生成碎片离子,过度裂解时将使待测物的分子量不易判定;使用较低的游离电压可以控制碎片离子的生成量,但离子的丰度低使得检测灵敏度降低。
EI的限制如下:
- 碎片过多造成质谱复杂,若分子离子不够稳定常有过度裂解的现象,不易决定分子量与结构。
- 不易分辨异构物。
- 试样游离之前需先汽化,故挥发度低的化合物不适用。
- 热不稳定化合物亦受加热挥发温度的限制。
(二) 化学游离法(chemical ionization, CI)
是一种通过离子-分子反应使样品离子化之方法,此离子化过程中主要利用试剂气体(Reagent gas)和气态待测物在离子源混合,因试剂气体的分压远高于气态待测物(约10000倍),故灯丝释出的电子主要撞击到试剂气体,使试剂气体先行游离,试剂气体离再与气态待测物碰撞使待测物游离,此种游离方式转移至待测物分子的能量较少,故生成的分子离子不易发生裂解,因此可提供待测物的分子量,常见的试剂气体有甲烷、氨、异丁烷及二甲基醚 (dimethyl ether, DME)。
以甲烷CH4为例:
- CH4经EI生成:CH4+、CH3+、CH2+、CH+等离子
CH4 + e- → CH4+、CH3+、CH2+、CH+、C+
- 上述离子与CH4形成具反应性的气态CH5+、C2H5+、C3H5+等离子。
- 具反应性的离子再与待测物分子碰撞结合或发生质子转移,而生成[M+1]+、[M+29]+与[M+41]+等离子。
一般而言,视试剂气体与待测物分子二者之质子亲和力(Proton affinity, PA)及热力学定律,进行下列四种可能的反应:
- 质子转移反应 M + XH+ → [M+H]+ + X
- 丛式结合反应 M + XH+ → [M+XH]+
- 电荷交换反应 M + XH+ → M+‧ + XH+‧
- 氢阴离子抽离反应 M + XH+ → [M-H]+ + XH2
<Note>
CI与EI比较:
- CI借由将能量透过试剂离子间接提供给样品分子,样品所获得能量较低,分子断裂的碎片较少,可克服因样品分子之碎片离子过多而侦测不到离子分子之困难,利于求得化合物之分子量。
- CI 由于试剂气体离子的背景值较高,使得灵敏度降低,且侦测极限通常较高。
- 两种游离法皆须使样品分子先加热气化,再进行气相碰撞反应,完成离子化过程。对于低挥发性、热不稳定以及高分子量之样品,均不适用。
八、(一) 说明以石墨炉原子吸收光谱仪(Graphite Furnace Absorption Spectrometry)测定饲料中重金属时,样品于测定前在石墨管中经过那些过程?
(二) 为何以石墨炉原子吸收光谱仪测定比火燄原子吸收光谱仪测定有较高的灵敏度?
解:
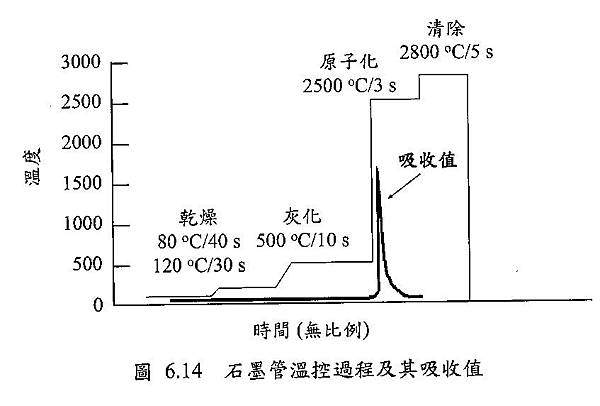
(一) 石墨炉原子吸收光谱仪(Graphite Furnace Absorption Spectrometry, GFAAS)以石墨管作为原子化器atomizer,样品滴入石墨管内的承接平台,经设定一石墨管升温程式,通过电流使石墨管渐次增加温度,升温阶段如下:在高流量氩气(Ar)下干燥阶段除去水份、灰化阶段破坏有机物,接著使用低流量Ar瞬间提升至欲分析元素的原子化温度取得分析讯号,最后再提升温度以清除石墨管。
(二)相较火焰式原子吸收光谱仪,GFAAS生成的自由气态原子在入射光径的滞留时间可达1秒以上,故灵敏度较高。